جمعبندی محاسبات اسیدها و بازها
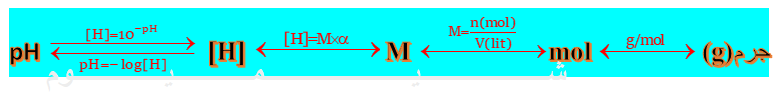
با توجه به فرمول بالا، با داشتن جرم یک اسید میتوان با استفاده از جرم مولی آن، به مول آن اسید رسید، و با توجه به حجم آن، به غلظت مولار آن اسید، و با استفاده از رابطۀ Mα به غلظت یون هیدرونیوم آن اسید رسیده و با log[H+] به pH آن اسید میرسیم؛ در حالت برعکس میتوان با استفاده از رابطۀ:
[H+]=10-pH
از pH یک اسید به غلظت یون هیدرونیوم آن برسیم، که این کار مستلزم یادگیری قوانین توان و لگاریتم است، که در زیر توضیح آنها آمده است:

برای مطالعۀ دقیقتر هر مطلب، به این صفحه مراجعه فرمایید.