سوال 105دفترچۀریاضی(سوال 30 شیمی)،اردیبهشت1403
نمودار زیر، تغییر غلظت مولی فراورده را برای واکنش: A(g)+D(g)⇌AD(g)، در دو شرایط متفاوت نشان میدهد،کدام مورد درست است؟ (P، فشار است.)
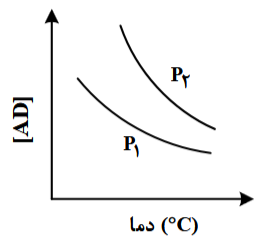
- P1<P2 و با کاهش دما، مقدار K واکنش افزایش مییابد.
- P2<P1 و با افزایش فشار، تعادل به سمت راست جابهجا میشود.
- P2<P1 و با کاهش دما، مقدار A و D، به یک نسبت تغییر میکند.
- P1<P2 و با افزایش حجم ظرف، غلظت گاز A و مقدار گاز AD افزایش مییابد.
پاسخ:
با توجه به نمودار، با افزایش دما، غلظت AD (فراورده) کاهش مییابد، پس طبق اصل لوشاتلیه با یک واکنش گرماده روبهرو هستیم، زیرا در یک واکنش گرماده (Q سمت فراورده وجود دارد) با افزایش دما، واکنش برای جبران گرمای زیادی، از Q دور شده و به سمت واکنش دهنده، پیشرفت میکند و به این صورت از غلظت فراورده (AD) کم میشود.
از طرفی تعداد مولهای گازی در سمت واکنش دهنده، بیشتر از مول گازی سمت فراورده است (2مول گازی در سمت واکنش دهنده و 1 مول گازی در سمت فراورده داریم). پس افزایش فشار (یا کاهش حجم) واکنش را به سمت تعداد مولهای کمتر (فشار کمتر) که همان فراورده است، جابهجا میکند.
حالا با این توضیحات بریم سراغ گزینهها:
1) P1<P2 و با کاهش دما، مقدار K واکنش افزایش مییابد:
درست است: در دمای ثابت، غلظت AD در منحنی بالا (مربوط به فشار P2) بیشتر از منحنی پایین (مربوط به فشار P1) است؛ از طرفی طبق توضیحات ابتدای پاسخ، با افزایش فشار، واکنش به سمت فشار کمتر (فراورده) پیشرفت کرده و غلظت فراورده افزایش مییابد؛ پس فشار P2 که غلظت بیشتری از فراورده (AD) را داراست، از فشار P1، بیشتر است.
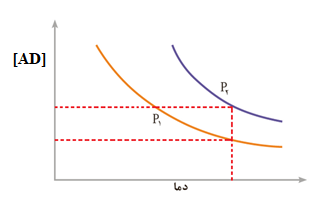
از طرفی به دلیل گرماده بودن واکنش، با کاهش دما، واکنش به سمت فراورده رفته و غلظت AD زیاد شده، در نتیجه K (ثابت تعادل) افزایش مییابد، زیرا ثابت تعادل، نسبت غلظت فراوردهها به واکنش دهندهها است.
2) P2<P1 و با افزایش فشار، تعادل به سمت راست جابهجا میشود:
نادرست است، زیرا: طبق توضیحات گزینۀ 1، P1<P2 بوده، ولی قسمت دوم گزینه درست است، زیرا با افزایش فشار، واکنش به سمت فشار کمتر (فراورده) پیشرفت میکند.
3) P2<P1 و با کاهش دما، مقدار A و D، به یک نسبت تغییر میکند:
نادرست است، زیرا: طبق توضیحات گزینۀ 1، P1<P2 بوده، اما قسمت دوم گزینه درست است، زیرا با کاهش دما، واکنش به سمت Q (که در سمت فراورده است،) رفته و از آنجایی که ضریب استوکیومتری A و D، با هم برابر است و هر دو واکنش دهنده هستند، غلظت آنها به یک نسبت کاهش خواهد یافت.
4) P1<P2 و با افزایش حجم ظرف، غلظت گاز A و مقدار گاز AD افزایش مییابد:
نادرست است، زیرا: ابتدای گزینه صحیح است که P1<P2 است، ولی با افزایش حجم (کاهش فشار)، واکنش به سمت فشار بیشتر (مولهای گازی بیشتر که همان واکنش دهندهها هستند،) رفته و مقدار فراورده (AD)، کاهش مییابد. از طرفی با افزایش حجم، غلظت مولی (مول حل شونده بر حجم محلول) تمامی مواد (چه واکنش دهنده و چه فراورده) کاهش خواهد یافت، هرچند که با توجه به اصل لوشاتلیه، واکنش در جهت برگشت رفته و مقداری از غلظت کم شدۀ واکنش دهندهها را جبران میکند.
بنابراین پاسخ گزینۀ 1 هست.
پیش نیاز لازم برای پاسخ به این تست:
- احاطه بر اصل لوشاتلیه
تحلیل سوال:
- این تست تمرین تازه اضافه شدۀ کتاب درسی بوده، ولی مورد جالب استفاده از 2 تست اصل لوشاتلیه در یک کنکور بود.
بخش زیبای تست:
- گزینۀ 4 که ارتباط بین حجم و غلظت را به چالش کشیده، از زیباییهای این تست بود.
بخش دوست نداشتنی تست:
- میتوانست نسبت به تمرین کتاب درسی در طراحی نمودار، کمی تغییر و تنوع داشته باشد.
برای دستیابی به نمره 20 امتحان نهایی و درصد بالای کنکور، به اندازۀ یک کلیک فاصله داری.