سوال 98 دفترچه (سوال 23 شیمی)رشته تجربی، تیر 1403
درباره سلول گالوانی استاندارد «آلومینیوم – هیدروژن»، کدام موارد زیر درست است؟
(حجم هر یک از محلولهای پیرامون آند و کاتد برابر یک لیتر است.)
(H=1,Al=27g.mol-1, E0(Al3+/Al)= -1.66 V)
الف: نسبت تغییرات جرم آند به تغییرات جرم کاتد، برابر 9 است.
ب: اگر غلظت H+(aq)، به اندازۀ 0.3 مولار کاهش یابد، غلظت Al3+(aq)، باید 0.9 مولار افزایش یابد.
پ: اگر 0.54 گرم از جرم آند کاسته شود، 672 میلی لیتر گاز هیدروژن در شرایط STP تشکیل شده است.
ت: در نمودار «مول-زمان» برای این سلول، شیب تغییر یون شرکت کننده در نیم واکنش کاتدی، 3 برابر شیب تغییر یون شرکت کننده در نیم واکنش آندی است.
- پ و ت
- ب و پ
- الف و ب
- الف و ت
پاسخ: با توجه به کمتر بودن E0 آلومینیوم نسبت به هیدروژن (SHE)، پس آلومینیوم را در آند و SHE را در کاتد قرار میدهیم، بدین صورت نیم واکنش آند و کاتد به صورت زیر خواهد بود:
Al(s)→Al3+(aq)+3e : نیم واکنش آندی (اکسایش)
2H+(aq)+2e→H2(g) : نیم واکنش کاتدی (کاهش)
حال برای اینکه الکترونها در نیم واکنشهای آندی و کاتدی با هم موازنه و برابر شوند، نیم واکنش آندی را در 2 ضرب میکنیم و نیم واکنش کاتدی را در 3 ضرب میکنیم تا در هر دو نیم واکنش، 6 تا الکترون داشته باشیم، و در این صورت واکنش کلی به صورت زیر خواهد شد:
2Al(s)+6H+(aq)→2Al3+(aq)+3H2(g)
حال به سراغ گزینهها میرویم:
الف: نسبت تغییرات جرم آند به تغییرات جرم کاتد، برابر 9 است:
نادرست است: چون الکترود موجود در نیم سلول SHE، جرم آن تغییری نمیکند، و چون در این گزینه، از واژۀ «تغییرات» استفاده شده، گزینه غلط است. توجه داشته باشیم که الکترود کاتد، هیدروژن نمیتواند باشد.
ب: اگر غلظت H+(aq)، به اندازۀ 0.3 مولار کاهش یابد، غلظت Al3+(aq)، باید 0.9 مولار افزایش یابد:
نادرست است زیرا: با توجه به اینکه حجم ظرف هر محلول 1 لیتری است، میتوانیم مولار را با مول برابر بگیریم، پس با توجه به واکنش کلی و استفاده از استوکیومتری خواهیم داشت:
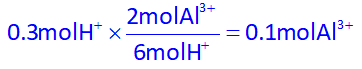
پس با مصرف 0.3 مولار H+(aq)، غلظت Al3+(aq) به اندازۀ 0.1 مولار، افزایش مییابد.
پ: اگر 0.54 گرم از جرم آند کاسته شود، 672 میلی لیتر گاز هیدروژن در شرایط STP تشکیل شده است:
درست است زیرا: طبق توضیحات ابتدای پاسخ، منظور از آند، فلز آلومینیوم است، پس با توجه به واکنش کلی و استفاده از استوکیومتری خواهیم داشت:

ت: در نمودار «مول-زمان» برای این سلول، شیب تغییر یون شرکت کننده در نیم واکنش کاتدی، 3 برابر شیب تغییر یون شرکت کننده در نیم واکنش آندی است:
درست است: شیب نمودار مول-زمان، همان سرعت است و میدانیم سرعت با ضریب استوکیومتری رابطۀ مستقیم دارد، از طرفی، یون شرکت کننده در نیم واکنش کاتدی، H+(aq) هست و یون شرکت کننده در نیم واکنش آندی، Al3+(aq) است، که در واکنش کلی، ضریب استوکیومتری یون هیدرونیوم، 6 بوده و ضریب استوکیومتری یون آلومینیوم، 2 هست، که نسبت آنها 3 میشود.
بنابراین جواب گزینۀ 1، (موارد پ و ت) خواهد بود.
پیش نیازهای لازم برای پاسخ به این تست:
- احاطه بر مبحث سلولهای گالوانی
- آشنایی با سینتیک
- احاطه بر استوکیومتری
تحلیل سوال:
- سلولهای الکتروشیمی، از مباحث اصلی کنکور محسوب میشوند که یادگیری مفهومی آنها از بایدهای داوطلبان کنکور است و در این تست از ترکیب آن با سینتیک و استوکیومتری به یک تست مفهومی رسیدیم.
بخش زیبای تست:
- گزینۀ 1، به زیبایی مفهوم آند و کاتد را به رخ میکشد.
بخش دوست نداشتنی تست:
- ندارد؛ تست جامعی بود، تبریک به طراح آن.