این log- را با p نشان میدهیم، پس:
pH یعنی log- غلظت یون هیدرونیوم:
pH= -log[H+]
و pOH یعنی log- غلظت یون هیدروکسید:
pOH= -log[OH–]
مثلا اگر غلظت یون هیدرونیوم اسیدی برابر با 5-10 مول بر لیتر باشد، pH آن برابر خواهد بود با:
[H+]=10-5
pH= -log10-5
pH= 5
همان طور که در مثال بالا میبینیم غلظت یون هیدرونیوم عدد بسیار کوچک و غیرقابل فهمی است، و با log- گرفتن از آن تبدیل به عدد قابل درکی میشود.
همچنین با استفاده از رابطۀ pH، میتوان از pH یک ماده، به غلظت یون هیدرونیوم آن رسید:
pH= -log[H+]
-pH=log[H+]
10 -pH = [H+]
در پستهای قبل متوجه شدیم که هرچه یک اسید قویتر باشد، غلظت یون هیدرونیوم آن بیشتر است، و با توجه به منفی داشتن لگاریتم در pH پس میتوان نتیجه گرفت که هرچه یک اسید قویتر باشد، دارای pH کمتری خواهد بود.
متقابلا هرچه یک باز قویتر باشد، غلظت یون هیدروکسید آن بیشتر است، و با توجه به منفی داشتن لگاریتم در pOH پس میتوان نتیجه گرفت که هرچه یک باز قویتر باشد، دارای pOH کمتری خواهد بود.
از طرفی با توجه به ثابت یونش آب میتوان نتیجه گرفت که:
pH+pOH=14
در نتیجه نمودار تغییرات pH به صورت زیر خواهد بود:
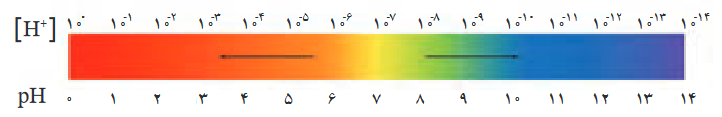
با توجه به نمودار بالا و توضیحات داده شده هرچه pH کمتر باشد محیط اسیدیتر بوده و هرچه pH زیادتر شود، محیط بازیتر خواهد شد.