در پیوند بین اتمی کوالانسی که بین دو نافلز رخ میدهد، برخلاف پیوند یونی، اتمها الکترون به اشتراک میگذارند و دیگر خبری از تبادل الکترون نیست.
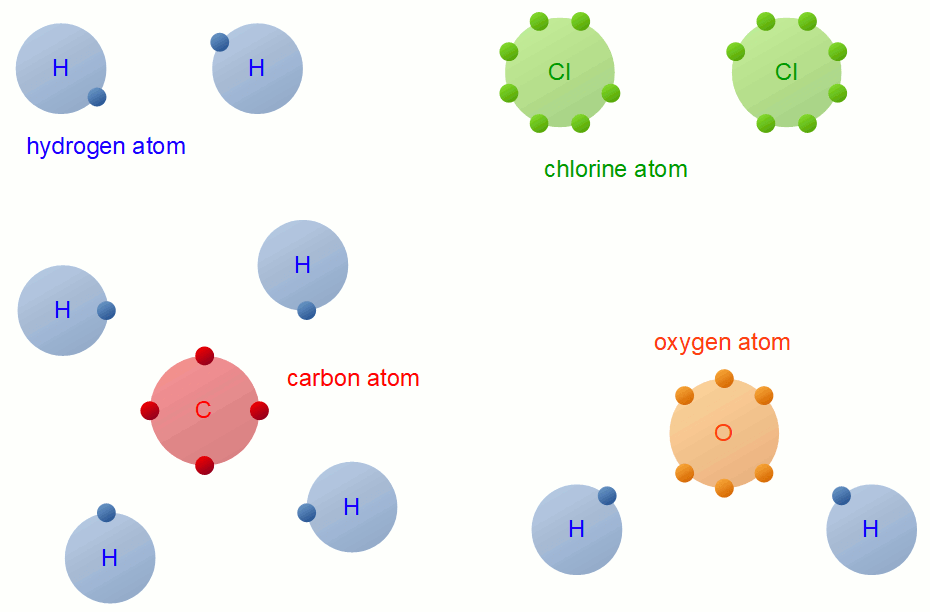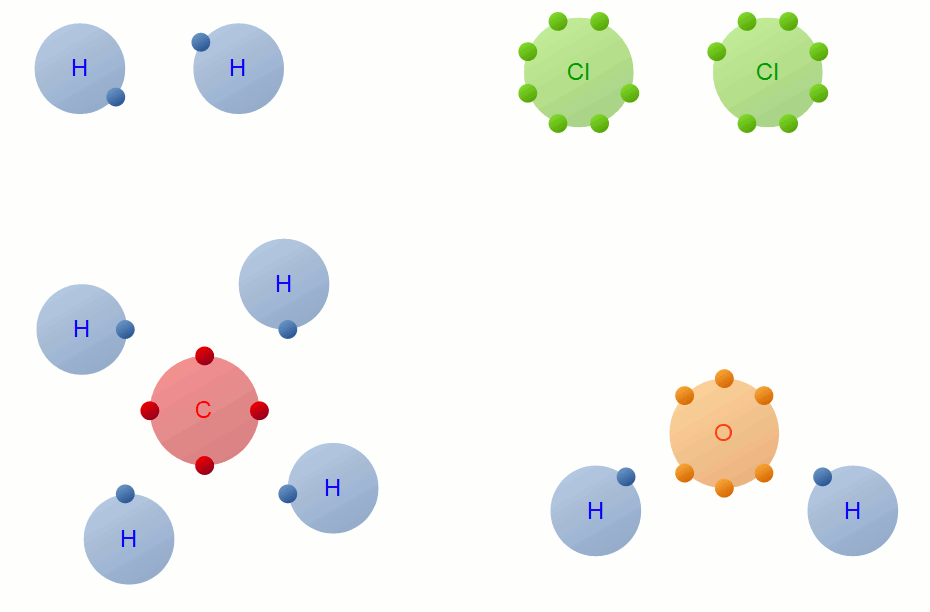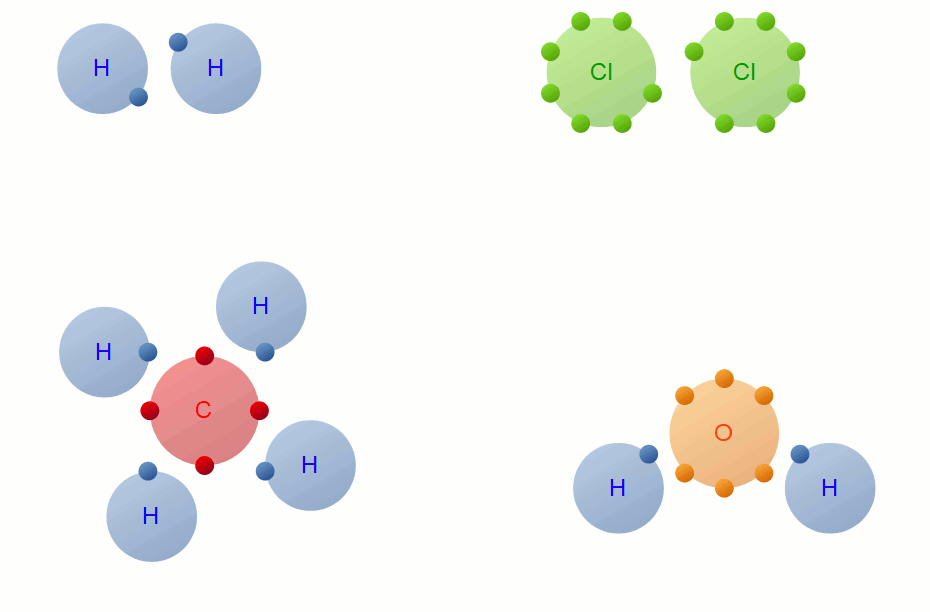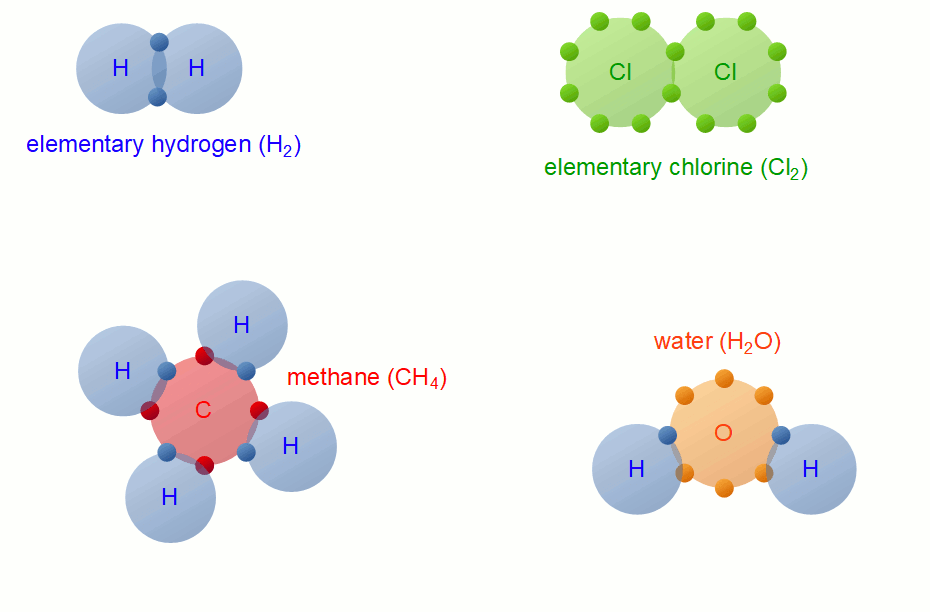
از آنجایی که شبه فلزها نیز از نظر واکنش پذیری شبیه به نافلزها عمل میکنند پس نیروی بین اتمی شبه فلزها با همدیگر یا با نافلزها از نوع کوالانسی خواهد بود. مثلا سیلیسیم (Si) که یک شبه فلز محسوب میشود، پیوند کوالانسی با اتم اکسیژن (که یک نافلز است) برقرار میکند.
اغلب ترکیبهایی که دارای نیروی بین اتمی کوالانسی هستند، مولکول تشکیل میدهند؛ کلمه اغلب به این معنا است که موادی وجود دارند که از یک شبکه بسیار غولپیکر با نیروی بین اتمی کوالانسی تشکیل شدهاند و اصولا جامد هستند، که اصطلاحا به این دسته از مواد، جامدات کوالانسی گویند.
در پست بعدی با جامدات کوالانسی آشنا خواهیم شد.
یک نظر
ترکیبکووالانسی تشکیل میدهند چون هر دو نافلزند