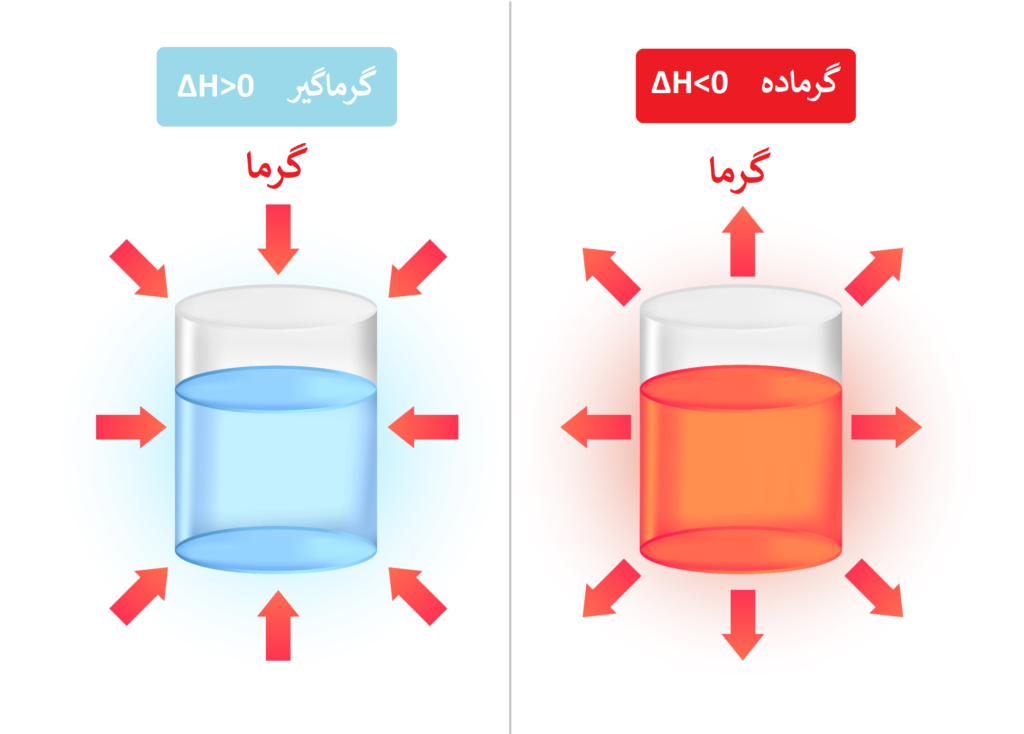
1) واکنشهای گرماگیر
2) واکنشهای گرماده
در پست قبل با مفاهیم سامانه، محیط و آنتالپی آشنا شدیم؛ همچنین گفته شد:
وقتی گرما از محیط به سامانه منتقل میشود سطح انرژی یا آنتالپی واکنش افزایش مییابد؛ و
زمانی که گرما از سامانه به محیط منتقل میشود سطح انرژی یا آنتالپی واکنش افزایش مییابد.
حال به آن دسته از واکنشها که گرما از محیط به سامانه منتقل شده، گرماگیر گوییم؛ و
آن دسته از واکنشها که گرما از سامانه به محیط منتقل میشوند را، گرماده گوییم.
پس میتوان گفت در واکنشهای گرماگیر، سطح انرژی فراوردهها از واکنش دهندهها بیشتر است، چون گرما از محیط به سامانه منتقل شده، و سامانه با دریافت گرما، سطح انرژی پایانی آن (یعنی فراوردهها) از سطح انرژی ابتدایی آن (یعنی واکنش دهنده) بیشتر خواهد شد.
همچنین میتوان گفت در واکنشهای گرماده، سطح انرژی واکنش دهندهها از فراوردهها بیشتر است، چون گرما از سامانه به محیط منتقل شده، و سامانه با از دست دادن گرما، سطح انرژی پایانی آن (یعنی فراوردهها) از سطح انرژی ابتدایی آن (یعنی واکنش دهنده) کمتر خواهد شد.
از طرفی در پست قبل متوجه شدیم که آنتالپی واکنش، برابر با اختلاف آنتالپی یا سطح انرژی فراوردهها فراوردهها و واکنش دهندهها است، یا:
ΔH=H2-H1
که در رابطۀ بالا ΔH همان آنتالپی واکنش بوده و H2 آنتالپی یا سطح انرژی فراوردهها میباشد و H1 آنتالپی یا سطح انرژی واکنش دهندهها محسوب میشود.
حال با استفاده از ΔH برای واکنشهای گرماگیر و گرماده، میتوان نتیجه گرفت که:
در یک واکنش گرماگیر، ΔH>0 هست یا آنتالپی واکنش مثبت میباشد، چون در واکنش گرماگیر، آنتالپی فراوردهها از آنتالپی واکنش دهندهها بیشتر است، پس اختلاف آنها که برابر با آنتالپی واکنش است، عددی مثبت خواهد بود؛
در یک واکنش گرماده نیز، ΔH<0 هست یا آنتالپی واکنش منفی میباشد، چون در واکنش گرماده، آنتالپی فراوردهها از آنتالپی واکنش دهندهها کمتر است، پس اختلاف آنها که برابر با آنتالپی واکنش است، عددی منفی خواهد بود.
اگر بخواهیم نمودار یک واکنش گرماگیر را بر حسب تغییرات آنتالپی نسبت به پیشرفت واکنش نشان دهیم (یعنی آنتالپی، محور y و پیشرفت واکنش، محور x باشد) به صورت زیر خواهد بود:
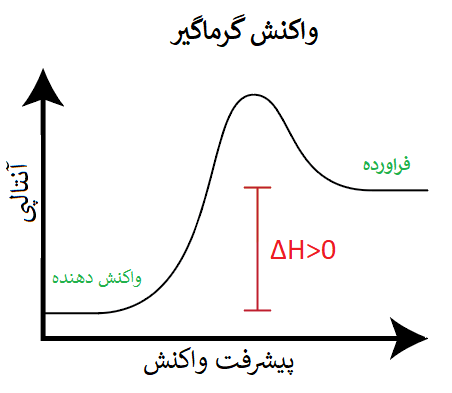
با توجه به توضیحات داده شده در مورد واکنشهای گرماگیر، نمودار بالا قابل قبول است، چون همان طور که گفته شد، در یک واکنش گرماگیر، سطح انرژی سامانه با دریافت گرما، افزایش یافته و آنتالپی پایانی (فراورده) بیشتر از آنتالپی آغازی (واکنش دهنده) خواهد بود.
همچنین اگر بخواهیم نمودار یک واکنش گرماده را بر حسب تغییرات آنتالپی، نسبت به پیشرفت واکنش نشان دهیم، به صورت زیر خواهد بود:
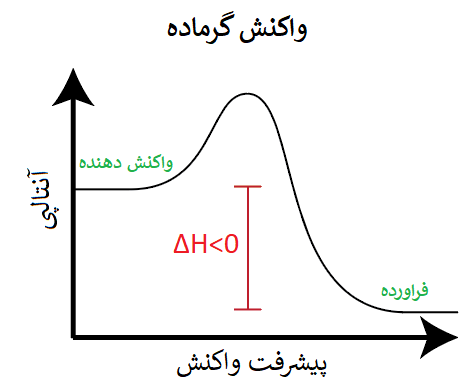
با توجه به توضیحات داده شده در مورد واکنشهای گرماده، نمودار بالا قابل قبول است، چون همان طور که گفته شد، در یک واکنش گرماده، سطح انرژی سامانه با از دست دادن گرما، کاهش یافته و آنتالپی پایانی (فراورده) کمتر از آنتالپی آغازی (واکنش دهنده) خواهد بود.
