پیوند هیدروژنی زمانی تشکیل میشود که اتم هیدروژن از یک مولکول به یکی از اتمهای FON (فلوئور، اکسیژن و نیتروژن) در مولکول دیگر متصل شود، مطابق شکل زیر:
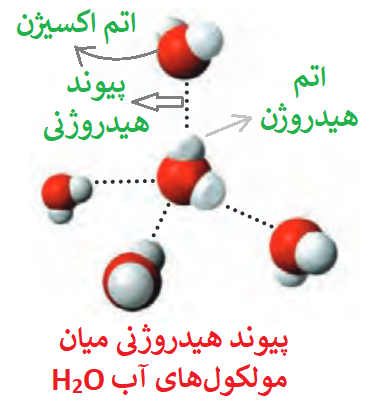
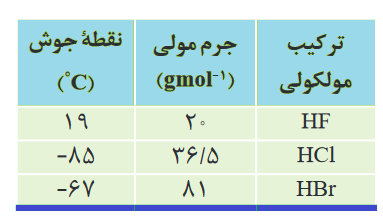
پیوند هیدروژنی قویترین نیرو، میان نیروهای بین مولکولی است به طوری که مولکولهای دارای پیوند هیدروژنی، نسبت به مولکولهای مشابه خود (همگروه خود) که پیوند هیدروژنی ندارند؛ نقطه جوش بالاتری دارند. مثلا در جدول زیر، نیروی بین مولکولی HF از نوع هیدروژنی است (زیرا اتم هیدروژن از یک مولکول HF به اتم فلوئور که یکی از اتمهای FON هست، در مولکول دیگر متصل شده است) پس نقطه جوش HF از مولکولهای همگروه خود (به خاطر داشتن پیوند هیدروژنی) همان طور که میبینیم خیلی بیشتر است.
دلیل قوی بودن پیوند هیدروژنی، میان نیروهای بین مولکولی، نیروی جاذبه زیاد بین هیدروژن و 3 اتم نامبرده (فلوئور، اکسیژن و نیتروژن) است.
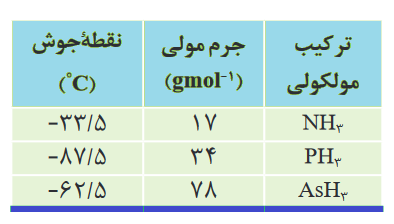
حال بین مولکولهای همگروهی که نیروی بین مولکولی آنها واندروالس است، مولکولی نقطه جوش بالاتری دارد که جرم مولی بیشتری داشته باشد. مثلا در جدول زیر بیشترین نقطه جوش را آمونیاک (NH3) دارد (چون بین مولکولی آن هیدروژنی است) و بعد از آن AsH3 نقطه جوش بیشتری از PH3 دارد، زیرا نیروی بین مولکولی آنها واندروالس است، پس مولکولی نقطۀ جوش بیشتری دارد که جرم مولی آن بیشتر است و از آنجایی که جرم مولی AsH3 از PH3 بیشتر است، پس نقطۀ جوش بیشتری دارد.
فراموش نکنیم موادی مولکول دارند که از نافلزها ساخته شدهاند و نیروی بین اتمی آنها کوالانسی هست، به عبارتی اغلب موادی که نیروی بین اتمی آنها کوالانسی هست، مولکول تشکیل میدهند. مانند تمام مواد بالا که اتمهای همگی نافلز هستند.