الکترولیت شامل نمکها، اسیدها و بازها میشود زیرا:
نمکها که ترکیبهای یونی بوده و در آب تفکیک شده و به یونهای سازندۀ خود تبدیل میشوند.
همچنین اسیدها و بازها در آب یونش پیدا کرده و به ترتیب یون هیدرونیوم و یون هیدروکسید در آب آزاد میکنند و آب را تبدیل به یک محلول الکترولیت میکنند.
متقابلا مادهای که در آب، یون آزاد نمیکند و به صورت مولکولی در آب حل میشود، مادۀ غیر الکترولیت گفته و به محلول آن، محلول غیرالکترولیت گوییم، مانند انحلال شکر در آب.
محلول الکترولیت، رسانای جریان برق بوده و اگر لامپی را با سیم در یک محلول الکترولیت قرار دهیم، آن لامپ روشن خواهد شد. مطابق شکل زیر:
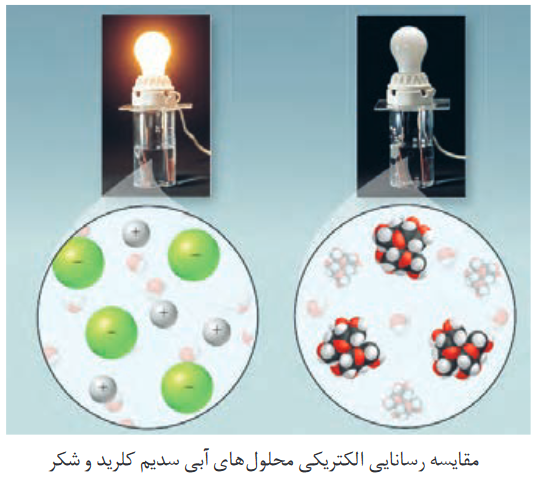
حال هر چقدر یونهای موجود در محلول الکترولیت بیشتر باشد و به عبارتی غلظت یونها بیشتر باشد، آن محلول الکترولیت، قویتر بوده و شاهد یک لامپ پرنورتر خواهیم بود.
مثلا با قرار دادن یک اسید ضعیف مانند HF و یک اسید قوی مانند HCl در دو ظرف مجزا، دو محلول الکترولیت خواهیم داشت، که یکی محلول الکترولیت ضعیف (محلول HF) و دیگری محلول الکترولیت قوی (محلول HCl) خواهد بود. مانند شکل زیر:
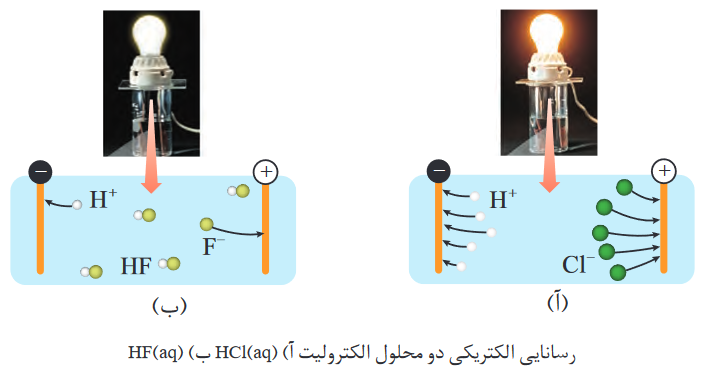
پس میتوان با توجه به توضیحات بالا متوجه شد که یونهای موجود در محلول HCl (که یک اسید قوی است) بیشتر از یونهای موجود در محلول HF (که یک اسید ضعیف است) خواهد بود؛ زیرا همان طور که گفته شد، هر چه تعداد یونها بیشتر باشد، لامپِ محلول الکترولیت، پرنورتر خواهد بود.
یک نظر
بله