اگر نیاز به مرور نحوه رسم ساختار لویس مواد را دارید، اینجا را کلیک کنید.
اگر اتم مرکزی آن ساختار دارای جفت الکترون ناپیوندی باشد، آن مولکول قطبی محسوب میشود، مانند مولکول اوزون (O3):
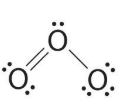
اما اگر اتم مرکزی آن ساختار، جفت الکترون ناپیوندی نداشته باشد آن ساختار را نمیتوان گفت که قطعا ناقطبی است، زیرا برای ناقطبی بودن یک مولکول باید ساختار لویس آن متقارن باشد، به بیان سادهتر باید اتمهای اطراف اتم مرکزی یکسان باشند، مانند مولکول زیر که یک مولکول ناقطبی محسوب میشود:
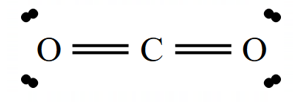
ولی در هر دو ساختار زیر، با وجود اینکه اتم مرکزی آنها جفت الکترون ناپیوندی ندارند، دی متیل اتر قطبی محسوب شده (زیرا اتمهای اطراف اتم مرکزی، یکسان نیستند و مولکول متقارن نیست) و پروپان ناقطبی محسوب میشود (زیرا اتمهای اطراف اتم مرکزی، یکسان هستند و مولکول متقارن است)
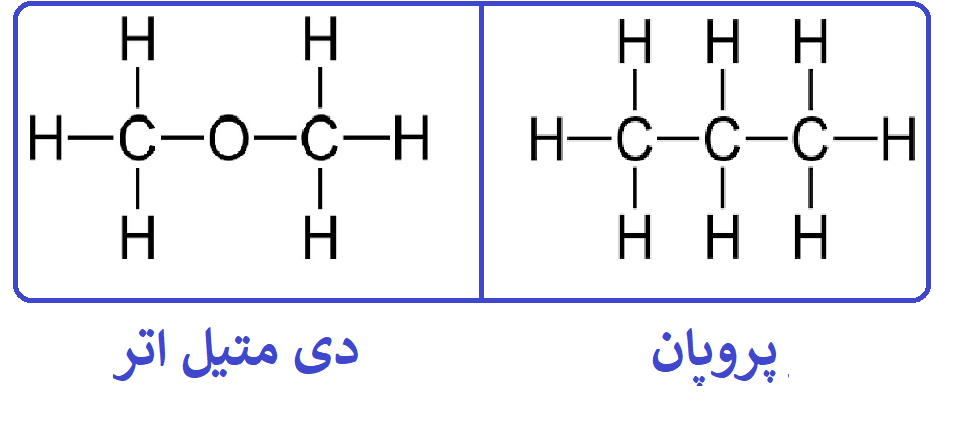
همچنین مولکولهای دو اتمی که از دو مولکول یکسان تشکیل شدهاند، متقارن بوده و ناقطبی محسوب میشوند، مثلا گاز اکسیژن از دو اتم اکسیژن تشکیل میشوند، پس گاز اکسیژن، ناقطبی است.
اما مولکولهای دو اتمی که از دو مولکول متفاوت تشکیل شدهاند، نامتقارن بوده و قطبی محسوب میشوند، مثلا HCl از دو اتم هیدروژن و کلر تشکیل میشوند، پس HCl، یک مولکول قطبی است.
همان طور که در پستهای قبل گفته شد به مولکولهای دو اتمی با اتمهای یکسان، مولکولهای جورهسته گوییم، و به مولکولهای دو اتمی با اتمهای متفاوت، مولکولهای ناجورهسته گفته میشود.
پس مولکولهای دو اتمی جورهسته، ناقطبی بوده و مولکولهای دو اتمی ناجورهسته، قطبی محسوب میشوند.
مولکولهای قطبی در یک میدان الکتریکی جهت گیری میکنند (منظم شده) و قسمت الکترونخواهتر (دارای بار جزئی منفی) آن به سمت صفحه مثبت میدان الکتریکی جهت میگیرد و قسمت کمتر الکترونخواه (دارای بار جزئی مثبت) آن به سمت صفحه منفی میدان الکتریکی جهت میگیرد.
مثلا HCl یک مولکول قطبی بوده که Cl به سمت صفحه مثبت میدان جهت میگیرد و H به سمت صفحه منفی میدان گرایش دارد.
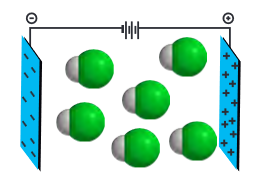
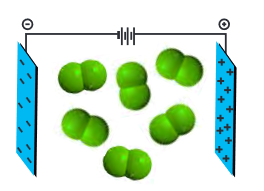
ولی مولکول F2 که یک مولکول ناقطبی هست در میدان الکتریکی جهتگیری نمیکند.
یک نظر
آب:قطبی
SO2:قطبی
So3:قطبی
NH3:قطبی
CH4:ناقطبی