در صورت نیاز به یادگیری روش به دست آوردن عدد اکسایش اتمها، به پست قبلی برگردید و در ادامه به مثال زیر توجه کنید:
مثال : محاسبه عدد اکسایش تمامی اتمها در واکنش زیر:
Cl2(g)+2HBr(aq)→Br2(aq)+2HCl(aq)
پاسخ:
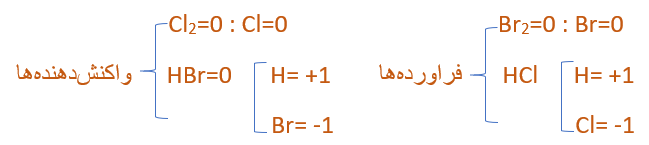
توضیح: در واکنش دهندهها چون که گاز کلر (Cl2) عنصر هست و خنثی هست پس عدد اکسایش آن برابر با صفر میشود، هیدروژنی هم که به Br متصل است، چون که به یک نافلز ترکیب شده، پس عدد اکسایش هیدروژن میشود: 1+ و ترکیب HBr برابر صفر قرار میدیم، پس عدد اکسایش Br میشود 1-
سمت فرآوردهها هم برم (Br2) عنصر هست، پس عدد اکسایش آن را برابر با صفر قرار میدهیم. و هیدروژن مجدداً به یک نافلز دیگر به اسم کلر متصل هست پس عدد اکسایش هیدروژن هم باز 1+ میشود، و وقتی عدد اکسایش HCl را برابر با صفر قرار دهیم؛ عدد اکسایش Cl هم میشود: 1-
همانطور که میبینیم عدد اکسایش Cl در سمت واکنش دهندهها برابر با صفر و در سمت فرآوردهها برابر با 1- میباشد، از طرفی عدد اکسایش Br در سمت واکنش دهندهها برابر با 1- و در سمت فرآوردهها برابر با صفر شده است؛ عدد اکسایش هیدروژن هم تغییری نکرده است. پس همانطور که میبینیم عدد اکسایش Cl کاهش یافته است، و عدد اکسایش Br افزایش یافته است، و اصطلاحا به آن ماده یا گونهای که عدد اکسایش آن در واکنش افزایش مییابد، میگوییم اکسایش یافته است.
به چنین واکنشهایی که در آنها، عدد اکسایش یک گونه، افزایش (اکسایش) یابد و عدد اکسایش گونه دیگر، کاهش یابد؛ سری واکنشهای اکسایش-کاهش گویند.
در پست بعدی در مورد گونههای اکسایش یافته و کاهش یافته بیشتر خواهیم آموخت.
یک نظر
سمت واکنش دهنده ها:
Fe:0. O2:0
فرآورده
Fe2O3:2fe+3(-2)=0. Fe=3