سوال 90 دفترچه (سوال 15 شیمی)تجربی، اردیبهشت1403
0.8 مول گاز A₂ و 2.4 مول گاز X2 وارد ظرف 2 لیتری دربسته میشود. اگر واکنش داده شده، با سرعت ثابت و در مدت ۱۰ دقیقه کامل شود، پس از چند دقیقه غلظت گاز X₂، برابر مجموع غلظت گازهای A2 و AX3 میشود و پس از این مدت، چند مول گاز در ظرف واکنش وجود خواهد داشت؟ (معادلۀ واکنش موازنه شود)
A2(g)+X2(g)→AX3(g)
1) 2.5 ، 1.2
2) 5 ، 1.2
3) 2.5 ، 2.4
4) 5 ، 2.4
پاسخ:
ابتدا واکنش را موازنه میکنیم:
A2(g)+3X2(g)→2AX3(g)
طبق شرایط سوال، فرض کنیم a مول از گاز A2، مصرف شده است؛ پس با استفاده از استوکیومتری خواهیم داشت:
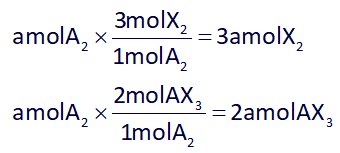
مطابق تست باید: غلظت باقیماندۀ گاز X2 را برابر با مجموع غلظت باقیماندۀ گاز A2 و غلظت تولیدی گاز AX3 قرار دهیم، بدین صورت مقدار a (مصرفی گاز A2) به دست میآید:

همان طور که میبینیم مقدار باقیمانده واکنش دهندهها نسبت به مقدار اولیه آنها نصف شده است، پس میتوان گفت با توجه ثابت بودن سرعت، وقتی کل واکنشدهندهها در 10 دقیقه مصرف میشوند، پس نصف آنها، در 5 دقیقه مصرف میشوند.
و در آخر مقدار کل گاز موجود در ظرف برابر است با، مقدار تولیدی فراورده و مقدار باقیمانده واکنشدهندهها:
1.2+0.4+0.8=2.4mol
بنابراین پاسخ گزینه 4 هست.
پیش نیاز لازم برای پاسخ به این تست:
- احاطه مبحث استوکیومتری و سینتیک
تحلیل سوال:
- پیش نیاز یادگیری مبحث سینتیک، احاطه بر مباحث استوکیومتری و غلظت هست که در این تست به وضوح مشخص بود.
بخش زیبای تست:
- برقراری ارتباط بین مواد باقیملنده و تولیدی از زیباییهای این تست بود.
بخش دوست نداشتنی تست:
- ندارد، فقط وجود غلظت و حجم داده شده (2 لیتر)، تاثیری در تست نداشت.