سوال 83 دفترچه (سوال 8 شیمی)تجربی، اردیبهشت1403
دربارۀ تهیۀ محلولهای رقیق از حلشونده مشابه در آب (شکلهای (۱) و (۲))، کدام مورد درست است؟ (از تغییر حجم در اثر اضافه کردن حلشونده صرفنظر شود.)
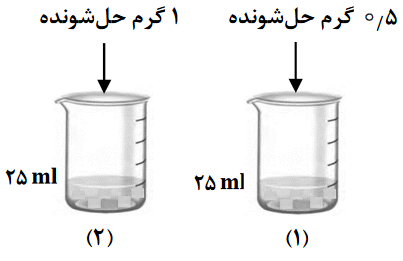
- تفاوت جرم محلول (۲) و جرم محلول (۱)، نصف جرم مولی حلشونده است.
- نسبت غلظت مولی حلشونده در دو ظرف، با نسبت درصد جرمی حلشونده در دو ظرف برابر است.
- اگر حجم حلال موجود در دو ظرف نصف شود، غلظت مولی حلشونده در ظرفها، به یک اندازه تغییر میکند.
- اگر محتویات دو ظرف به یکدیگر اضافه شوند، درصد جرمی محلول حاصل، 3 برابر درصد جرمی محلول (۱) خواهد بود.
پاسخ:
با فرض اینکه چگالی آب 1 گرم بر میلیلیتر بوده (25 میلیلیتر آب را برابر با 25 گرم در نظر میگیریم) و اضافه شدن حلشونده منجر به افزایش جرم مایع میشود به سراغ گزینهها میرویم:
1) تفاوت جرم محلول (۲) و جرم محلول (۱)، نصف جرم مولی حلشونده است:
نادرست است: با توجه به برابر بودن جرم حلال (آب) در هر دو ظرف، تفاوت جرم محلول (۲) و جرم محلول (۱) برابر است با:
(25+1)-(25+0.5)=0.5g
جرم مولی حل شونده داده نشده است تا با پاسخ مقایسه کنیم.
2) نسبت غلظت مولی حلشونده در دو ظرف، با نسبت درصد جرمی حلشونده در دو ظرف برابر است:
تقریبا درست است: با توجه به اینکه در صورت سوال آمده که با اضافه شدن حلشونده حجم محلول تغییری نمیکند، پس حجم محلول را برابر با حجم حلال (25ml) قرار داده و نسبت غلظت مولی حلشونده در دو ظرف به دست میآوریم:

حال از آنجایی که درصد جرمی برابر با جرم حلشونده به جرم محلول است، با داشتن جرم حلشوندهها و جرم محلولها (جرم حلال+حلشونده) نسبت درصد جرمی در دو ظرف را به دست میآوریم:
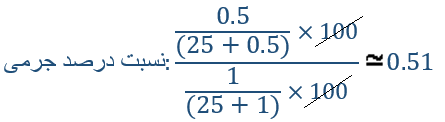
که به طور تقریبی نسبت غلظت مولی با نسبت غلظت جرمی برابر است.
3) اگر حجم حلال موجود در دو ظرف نصف شود، غلظت مولی حلشونده در ظرفها، به یک اندازه تغییر میکند:
نادرست است: با توجه به اینکه حجم حلال با حجم محلول برابر است، در فرمول غلظت مولی، مخرج کسر برابر با حجم محلول است، با نصف شدن حجم حلال، مخرج کسر غلظتهای مولی نصف شده و به یک نسبت غلظت مولی هر دو ظرف افزایش مییابد، نه به یک اندازه:

4) اگر محتویات دو ظرف به یکدیگر اضافه شوند، درصد جرمی محلول حاصل، 3 برابر درصد جرمی محلول (۱) خواهد بود:
نادرست است: با افزوده شدن محتویات دو ظرف به همدیگر، جرم حلشونده ها با هم جمع میشود:
0.5+1=1.5g
حجم محلول جدید برابر با مجموع جرم دو محلول خواهد بود:
(25+0.5)+(25+1)=51.5g محلول جدید
درصد جرمی هم برابر است با نسبت جرم حلشونده به محلول، و نسبت درصد جرمی محلول جدید 3 برابر درصد جرمی محلول (۱) نیست:
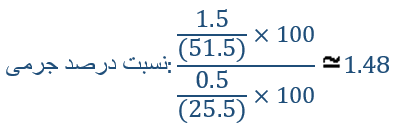
بنابراین پاسخ گزینه 1 هست.
پیش نیاز لازم برای پاسخ به این تست:
- احاطه بر مبحث غلظت مولار
- احاطه بر مبحث درصد جرمی
تحلیل سوال:
- سوالهای ترکیبی غلظتها از تستهای اغلب کنکورهای چند سال اخیر بوده که پیشنیاز تسلط بر آنها، احاطه بر مفهوم محلول هست.
بخش زیبای تست:
- مقایسۀ غلظتها و اجزای آنها (حلال و حلشونده) با همدیگر، در هر گزینه، از زیبایی این تست بود.
بخش دوست نداشتنی تست:
- متاسفانه این تست یکی از مبهمترین تستهای چند سال اخیر بود:
- ابهام 1: جرم مولی حلشونده داده نشده ولی در گزینۀ 2 از آن سوال پرسیده میشود.
- ابهام 2: وقتی از افزایش حجم حلشونده صرف نظر میکنیم، باید در مورد افزایش جرم قید شود که باید لحاظ گردد (حداقل 20 نفر از شاگردان خودم این سوال رو ازم پرسیدن)
- ابهام 3: هر چند بدون قید شدن چگالی آب، درصدجرمی محلولها قابل محاسبه بود ولی با عدم ذکر مقدار عددی چگالی آب، ابهامی دیگر در ذهن داوطلب کنکور شکل میگیرد.
- ابهام 4: گزینۀ 2، که گزینۀ صحیح است، اعداد دو نسبت غلظتهای مولی و جرمی دقیق یکی نیست. (با در نظر گرفتن ابهام 5)
- ابهام 5: 25ml موجود در دو ظرف مربوط به قبل از افزودن حلشونده هست یا بعد از آن؟! (برای غلظت مولی فرقی ندارد با توجه به صرفنظر کردن از حجم حلشونده) ولی در بحث درصد جرمی همان طور که دیدیم مهم است، ما این تست را با حالت قبل از افزودن حلشونده جلو بردیم؛ چرا: چون مقدار عددی چگالی را برای آب خالص (حلال) در نظر گرفتیم.
مورد جالب:
- با رفع این ابهامات، این تست به یکی از زیباترین تستهای این کنکور تبدیل میشد.

2 نظر
بسیار ممنونم از تحلیل بسیار عالی شما
در هیچ ویدئویی تحلیلی انقدر دقیق پیدا نکردم
این تست از تست هایی بود که همیشه برایم گنگ بود ولی به لطف تحلیل شما برایم شفاف شد سپاس
افتخاری برای بنده هست دیدگاه شما.