با توجه به واکنش زیر ۲۰۰ گرم محلول سولفوریک اسید ۴.۹ درصد جرمی با چند گرم فلز آهن واکنش کامل میدهد؟(معادله واکنش موازنه شود، H=1 , O=16 , S=32 , FE=56 : g.mol-1)
H2SO4(aq)+Fe(s)→FeSO4(aq)+SO2(g)+H2O(l)
1) 1.4
2) 2.8
3) 5.6
4) 11.2
ابتدا معادله را موازنه میکنیم:
2H2SO4(aq)+Fe(s)→FeSO4(aq)+SO2(g)+2H2O(l)
حال مقدار خالص سولفوریک اسید (H2SO4(aq)) را به دست میآوریم:
200gH2SO4×0.049=9.8gH2SO4 خالص
اکنون با استفاده از استوکیومتری، از مقدار خالص سولفوریک اسید به مقدار آهن میرسیم:
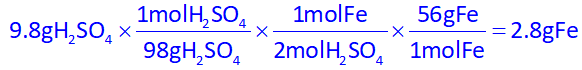
توجه به مبحث درصد جرمی در سری سوالات استوکیومتری در این تست خودنمایی میکرد.
اینکه طراح تست دو واکنش دهنده را هدف سوال خود قرار داده بود جالب بود. (غالبا از یک واکنش دهنده و یک فراورده در استوکیومتری بحث میشود)
سطح سوال پایین بود که البته توجیه دارد: این تست برای مدیریت زمان لازم بود.