سوال 81 دفترچه (سوال 6 شیمی)رشته تجربی، تیر 1403
اگر 22.5 گرم اوره در 727.5 گرم آب مقطر حل شود، غلظت مولی آن کدام است؟ (جرم هر میلیلیتر محلول، برابر یک گرم در نظر گرفته شود. H=1, C=12, N=14, O=16 : g.mol−1)
۱) 1
۲) 0.5
۳) 0.75
۴) 1.25
پاسخ:
فرمول اوره برابر با CO(NH2)2 هست پس جرم مولی 22.5 گرم از آن به صورت زیر است:
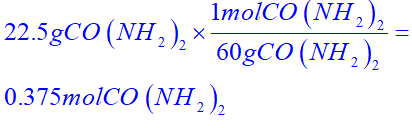
حجم محلول نیز برابر حجم آب خالص و اوره، به صورت زیر است:
22.5+727.5=750g محلول
با توجه به صورت سوال، جرم هر میلیلیتر محلول، برابر یک گرم است، پس 750 گرم محلول، برابر با 0.750 میلی لیتر محلول است.
پس غلظت مولی که نسبت مول حل شونده (اوره) به حجم محلول است، برابر خواهد بود با:
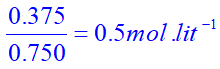
بنابراین پاسخ گزینۀ 2 خواهد بود.
پیش نیازهای لازم برای پاسخ به این تست:
- آشنایی با مبحث استوکیومتری
- آشنایی با نام مواد
- احاطه بر مبحث غلظت مولار
تحلیل سوال:
- آشنایی با نام مواد از این جهت حائز اهمیت است که در صورت احاطه بر مبحث غلظت و استوکیومتری، اگر فرمول اوره را نمیدانستیم این تست قابل حل نبود.
بخش زیبای تست:
- تبدیل جرم محلول به حجم، از قسمتهای زیبای این تست بود.
بخش دوست نداشتنی تست:
- ندارد، فقط برای زیباتر شدن تست میشد از واکنش شیمیایی و استوکیومتری استفاده کرد.