نافلزها تمایل به گرفتن الکترون دارند، واکنشپذیری نافلزها با شعاع اتمی رابطۀ عکس دارد، به عبارتی هرچه شعاع اتمی کمتر باشد تمایل به نافلز بودن بیشتر است، و از آنجایی که در یک دوره با افزایش عدد اتمی، شعاع اتمی کاهش مییابد، پس تمایل به نافلز بودن افزایش خواهد یافت؛ و در یک گروه از بالا به پایین، چون شعاع اتمی افزایش مییابد پس تمایل به نافلز بودن کاهش خواهد یافت.
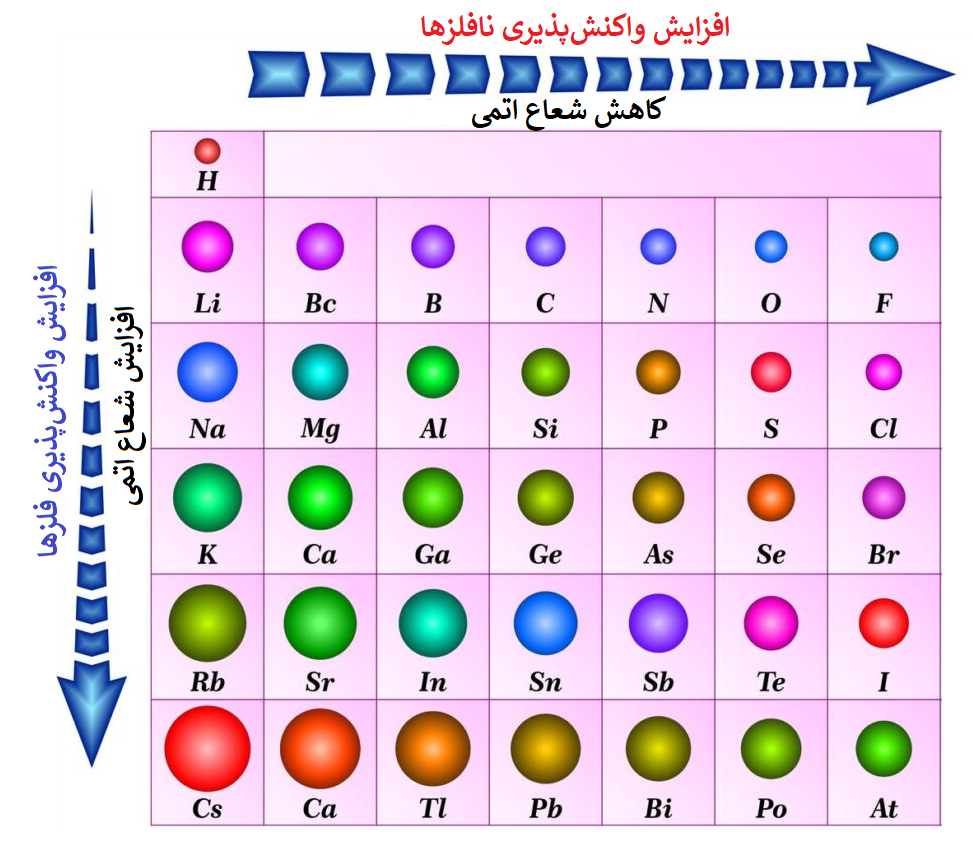
موردی که جالب است اینجاست که اگر بگوییم مطلقا در یک دوره با افزایش عدد اتمی، خصلت و واکنشپذیری نافلزها افزایش مییابد جملهی اشتباه خواهد بود، زیرا آخرین گروه که در راستترین قسمت جدول دورهای واقع شده است گازهای نجیب هستند (گروه 18 یا گروه 8 اصلی) و گازهای نجیب تمایلی به واکنش ندارند و پایدارند، پس واکنشپذیری نافلزها تا گروه 17 یاگروه 7 اصلی ادامه دارد، مطابق نمودار زیر:
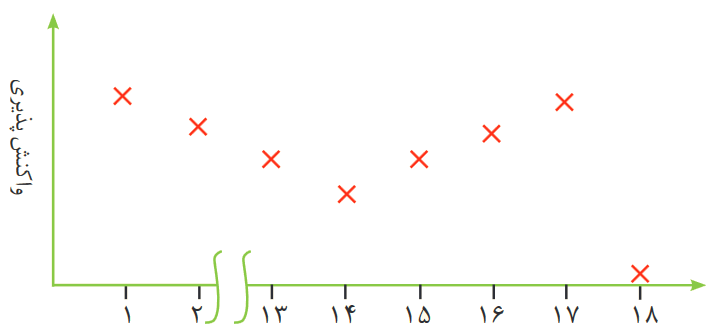
همان طور که در نمودار بالا مشاهده میکنیم واکنشپذیری عناصر ابتدا کاهش مییابد و سپس افزایش مییابد، البته تا گروه 17. دلیل کاهش واکنشپذیری در ابتدا این است که:
در یک دوره، شعاع اتمی کاهش مییابد و از آنجایی که عناصر سمت چپ فلز هستند، با کاهش شعاع اتمی، واکنش پذیری آنها کاهش مییابد (زیرا فلزها تمایل به از دست دادن الکترون دارند) ولی از گروه 14 یا 4 اصلی عناصر نافلز میشوند، و با کاهش شعاع اتمی، واکنش پذیری آنها افزایش خواهد یافت (زیرا نافلزها تمایل به گرفتن الکترون دارند و با کاهش شعاع اتمی تمایل به گرفتن الکترون افزایش مییابد)، به همین خاطر نمودار از گروه 14 به بعد رو به بالا میرود تا گروه 17 یا 7 اصلی. ولی دلیل اینکه واکنشپذیری در گروه 18 یا 8 اصلی بسیار کم میشود این است که گازهای نجیب در گروه 8 قرار دارند و با توجه به آرایش الکترونی آنها، تمایلی به واکنشپذیری ندارند.
یک نظر
F زیرا از چپ به راست واکنش پذیری نافلز ها در جدول تناوبی افزایش می یابد