خود را بیازمایید صفحه16 شیمی دوازدهم
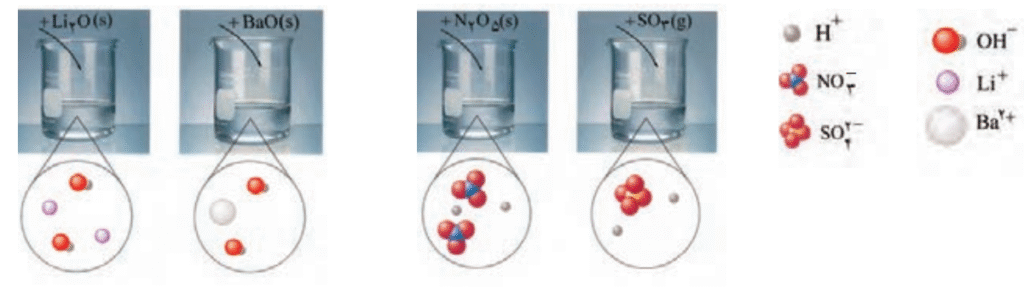
آ) برخی اکسیدها با آب واکنش میدهند. با توجه به شکل زیر مشخص کنید اکسیدی که وارد آب میشود، اسید آرنیوس است یا باز آرنیوس؟ چرا؟
پاسخ:
به طور کلی، غالبا اکسید فلزها در آب، باز آرنیوس محسوب میشوند، زیرا با حل شدن در آب، یون هیدروکسید (–OH) آزاد میکنند؛ و اکسید نافلزها، اسید آرنیوس محسوب میشوند، زیرا در آب، یون هیدرونیوم (+H) آزاد میکنند. پس:
Li2O : باز آرنیوس
BaO : باز آرنیوس
N2O5 : اسید آرنیوس
SO3 : اسید آرنیوس
ب) معادلۀ شیمیایی واکنش هر یک از این اکسیدها را با آب بنویسید و موازنه کنید.
پاسخ:
در پایین، معادله حل شدن در آب و سپس یونش هر اکسید را مینویسیم:
- Li2O (اکسید فلزی، باز)
Li2O(s)+H2O(l)→2LiOH(aq) حل شدن
LiOH(aq)→Li+(aq) + OH−(aq) یونش
- BaO (اکسید فلزی، باز)
BaO(s)+H2O(l)→Ba(OH)2(aq) حل شدن
Ba(OH)2(aq)→Ba2+(aq) + 2OH−(aq) یونش
- N2O5 (اکسید نافلزی، اسید)
N2O5(g)+H2O(l)→2HNO3(aq) حل شدن
HNO3(aq)→H+(aq) + NO3−(aq) یونش
- SO3 (گاز) (اکسید نافلزی، اسید)
SO3(g)+H2O(l)→H2SO4(aq) حل شدن
H2SO4(aq)→H+(aq) + HSO4−(aq) یونش
پ) جدول زیر را کامل کنید.
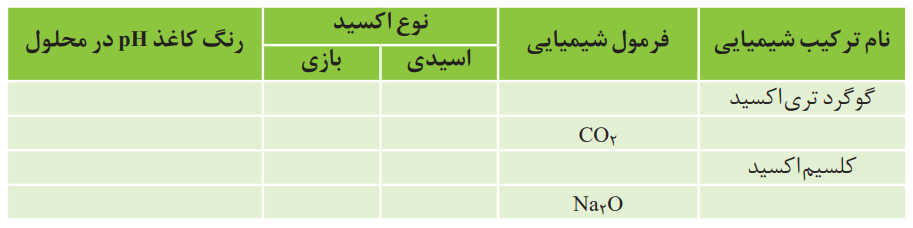
| نام ترکیب شیمیایی | فرمول شیمیایی | نوع اکسید | رنگ کاغذ pH در محلول |
|---|---|---|---|
| گوگرد تریاکسید | SO3 | اسیدی | قرمز |
| کربن دیاکسید | CO2 | اسیدی | قرمز |
| کلسیم اکسید | CaO | بازی | آبی |
| سدیم اکسید | Na2O | بازی | آبی |
برای درک بهتر خودآزمایی بالا، این پست را مطالعه فرمایید یا در این آزمون رایگان شرکت کنید.