جمعبندی اعداد کوانتومی و آرایش الکترونی
اعداد کوانتومی در حد شیمی دبیرستان به دو مورد: n (عدد کوانتومی اصلی) و l (عدد کوانتومی فرعی) تقسیم میشوند که:
n نشان دهندۀ شمارۀ لایه است و از 1 تا 7 میباشد، مطابق شکل زیر:
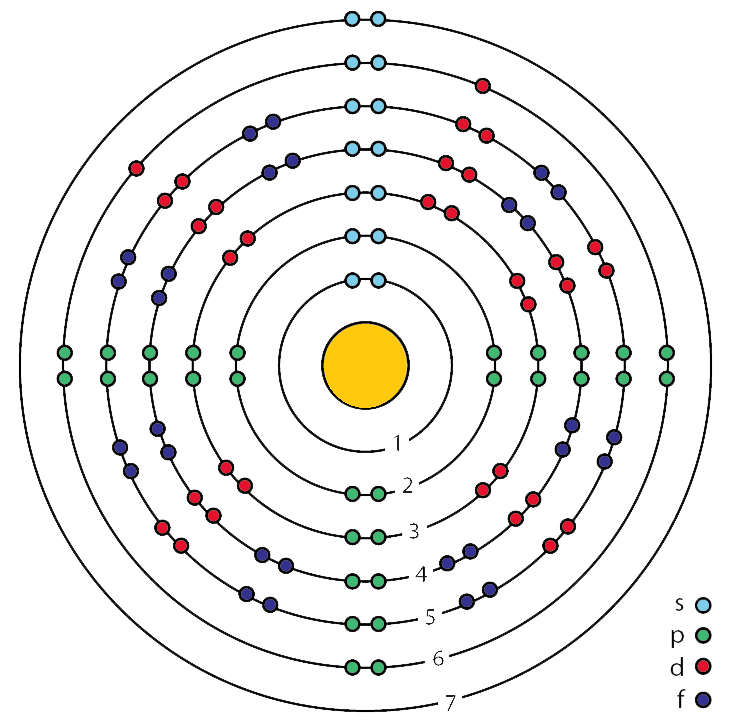
و l نشان دهندۀ نوع زیرلایه هست که:
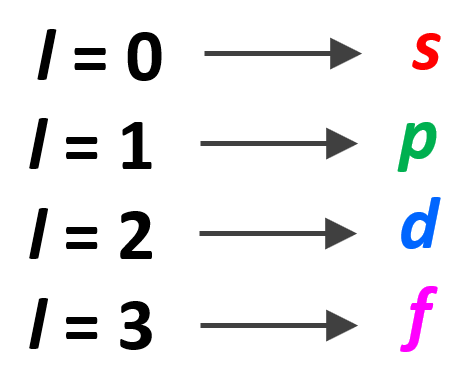
پس اگر l=0 باشد، زیرلایه از نوع s هست، که نهایتا 2 الکترون در آن جای میگیرد.
اگر l=1 باشد، زیرلایه از نوع p هست، که نهایتا 6 الکترون در آن جای میگیرد.
اگر l=2 باشد، زیرلایه از نوع d هست، که نهایتا 10 الکترون در آن جای میگیرد.
اگر l=3 باشد، زیرلایه از نوع f هست، که نهایتا 14 الکترون در آن جای میگیرد.
که نمایش اعداد کوانتومی در حالت آرایش الکترونی به صورت زیر است:
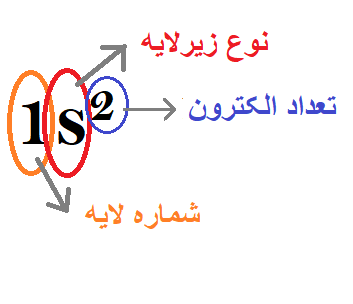
که در نوشتن آرایش الکترونی:
همیشه هر لایه با زیرلایۀ s شروع شده و با زیرلایۀ p تمام میشود.
بعد از پر شدن زیرلایۀ p (گرفتن 6 الکترونش)، زیرلایۀ s لایه بعد را مینویسیم، مثلا بعد از 2p6 باید زیرلایه s لایۀ بعدی را بنویسیم که میشود: 3s2
زیرلایه 3d را بعد از 4s2 مینویسیم، با اینکه یک لایه پایینتر از 4s قرار دارد. (به دلیل انرژی زیاد زیرلایۀ d نسبت به زیرلایۀ s)
پس آرایش الکترونی عناصر تا عنصر 36 (36Kr) خواهد بود:

به عنوان مثال آرایش الکترونی تیتانیوم (22Ti) به صورت زیر خواهد بود:
22Ti : 1s2 2s2 2p6 3s2 3p6 4s2 3d2
توجه: در حالت خنثی، آرایش الکترونی 3d4 و 3d9 نداریم، پس آرایش الکترونی 24Cr و 29Cu که به این زیرلایهها (3d4 و 3d9) ختم میشوند، به صورت زیر خواهند بود:
24Cr : 1s2 2s2 2p6 3s2 3p6 4s2 3d4 => 1s2 2s2 2p6 3s2 3p6 4s1 3d5
29Cu : 1s2 2s2 2p6 3s2 3p6 4s2 3d9 => 1s2 2s2 2p6 3s2 3p6 4s1 3d10
آرایش الکترونی فشرده (با استفاده از گاز نجیب):
گازهای نجیب موردنیاز برای استفاده از آنها در آرایش الکترونی فشرده به صورت زیر هستند:

روش نوشتن آرایش الکترونی فشرده به این صورت است که با توجه به تعداد الکترونهای عنصر داده شده، نماد گاز نجیب قبل از آن عنصر را مینویسیم و آرایش الکترونی، الکترونهای باقیمانده را اضافه میکنیم. مثلا سدیم (11Na) در حالت خنثی 11 تا الکترون دارد، پس نزدیکترین گاز نجیبی که قبل از آن، قرار دارد نئون (10Ne) هست، در نتیجه مینویسیم:
11Na:[Ne]
ولی هنوز 1 الکترون دیگر نیاز داریم (چون سدیم 1 الکترون بیشتر از نئون دارد) و از آنجایی که آرایش الکترونی نئون به 2p6 ختم میشود، همان طور که بالاتر توضیح داده شد، بعد از زیرلایۀ p، زیرلایۀ s لایۀ بعدی را مینویسیم، در نتیجه بعد 2p6 مینویسیم: 3s و چون فقط 1 الکترون لازم داریم تا بعد از آرایش الکترونی نئون به آرایش الکترونی سدیم برسیم، میشود:
11Na:[Ne]3s1
برای مطالعۀ دقیقتر، پستهای مرتبط در این لینک را مطالعه فرمایید.