دوره در جدول تناوبی به معنی آخرین لایۀ اشغال شده از الکترون است، پس وقتی میگوییم یک دوره یعنی یک لایه، در نتیجه لایه ثابت است و تغییر نمیکند.
پس دلیل اینکه تغییرات شعاع اتمی در یک دوره با کاهش همراه است این هست که در یک لایه با افزایش عدد اتمی، بار موثر هسته یا جاذبه کشش الکترونها به سمت هسته، افزایش یافته و این گونه شعاع اتمی عناصر کاهش مییابد.
عدد اتمی هم که همان تعداد پروتونها است و میدانیم در یک دوره (یا یک لایه) از چپ به راست عدد اتمی یکی یکی زیاد میشود.
مثلا روند تغییرات شعاع اتمی عناصر دسته اصلی در دوره سوم به صورت زیر است:
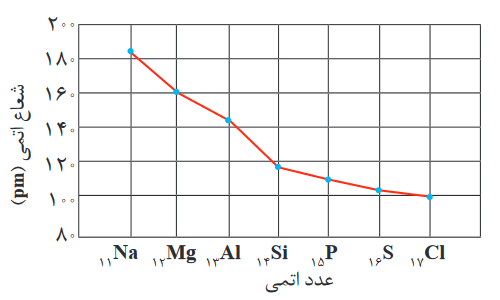
دلیل روند شعاع اتمی در نمودار بالا همان طور که گفته شد این است که در یک دوره با افزایش عدد اتمی، شعاع اتمی کاهش مییابد؛ و چون بیشترین عدد اتمی مربوط به کلر (17Cl) است، پس کمترین شعاع مربوط به کلر میشود.
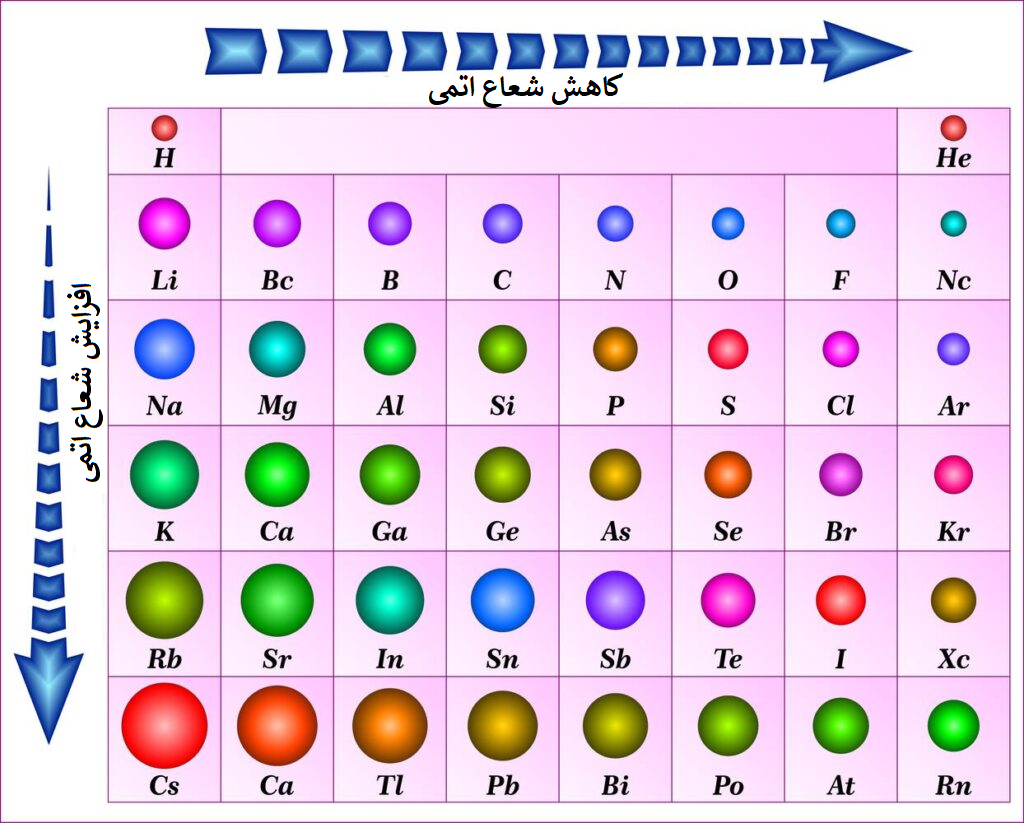
حال که در پست قبلی متوجه شدیم در یک گروه با افزایش عدد اتمی، شعاع اتمی عناصر بزرگ میشود و در این پست فهمیدیم در یک دوره با افزایش عدد اتمی، شعاع عناصر کاهش مییابد؛ میتوانیم جدول زیر را درک کنیم:
یک نظر
Li بیشترین شعاع اتمی و Ne کمترین شعاع اتمی زیرا در یک دروه از چپ به راست شعاع اتمی کاهش می یابد