باهمبیندیشیم صفحه40 شیمی3
اکسیژن نافلزی فعال است که با اغلب فلزها واکنش میدهد و آنها را به اکسید فلز تبدیل میکند، درحالی که با برخی فلزها مانند طلا و پلاتین واکنش نمیدهد. شکل زیر الگوی سادهای از واکنش بین اتمهای روی و اکسیژن را با ساختار لایهای اتم نشان میدهد.
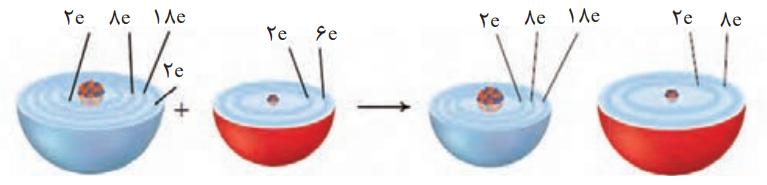
آ) کدام ساختار، اتم روی و کدام یک، اتم اکسیژن را نشان میدهد؟
پاسخ:
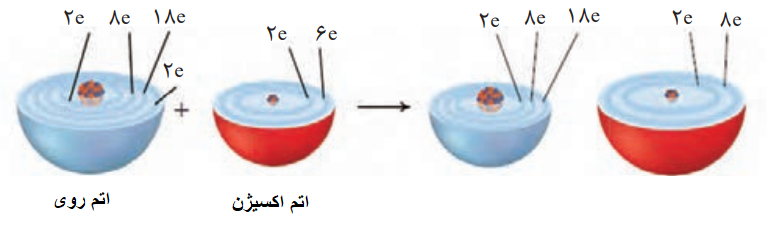
ب) کدام اتم الکترون از دست داده و کدام الکترون گرفته است؟
پاسخ:
اتم روی الکترون از دست داده و تبدیل به یون روی (+Zn2) میشود و اتم اکسیژن الکترون گرفته و تبدی به یون اکسیژن (–O2) میشود.
پ) اگر گرفتن الکترون را کاهش و از دست دادن الکترون را اکسایش بنامیم، کدام گونه کاهش و کدام اکسایش یافته است؟
پاسخ:
اتم اکسیژن که الکترون گرفته، کاهش یافته و اتم روی که الکترون از دست داده، اکسایش یافته است.
ت) شیمیدانها هریک از فرایندهای گرفتن و از دست دادن الکترون را با یک نیمواکنش نمایش میدهند که هر نیمواکنش باید از لحاظ جرم (اتمها) و بار الکتریکی موازنه باشد. اینک با قرار دادن شمار معینی الکترون، هریک از نیمواکنشهای زیر را موازنه کنید.
Zn(s)→Zn2+(s)+…..
O2(g)+……→۲O2−(s)
پاسخ:
Zn(s)→Zn2+(s)+2e
O2(g)+4e→۲O2−(s)
ث) کدام یک از نیمواکنشهای بالا، نیمواکنش اکسایش و کدام یک نیمواکنش کاهش را نشان میدهد؟ چرا؟
پاسخ:
Zn(s)→Zn2+(s)+2e نیم واکنش اکسایش است، زیرا اتم روی الکترون از دست داده است.
O2(g)+4e→۲O2−(s) نیم واکنش کاهش است، زیرا اتم اکسیژن الکترون گرفته است.
ج) مادهای که با گرفتن الکترون سبب اکسایش گونۀ دیگر میشود، اکسنده و مادهای که با دادن الکترون سبب کاهش گونۀ دیگر میشود، کاهنده نام دارد. در واکنش روی با اکسیژن، گونۀ اکسنده و کاهنده را مشخص کنید.
پاسخ:
اتم اکسیژن، گونۀ اکسنده هست، زیرا با گرفتن الکترون سبب اکسایش اتم روی میشود. و اتم روی، گونۀ کاهنده هست، زیرا با از دست دادن الکترون، سبب کاهش اتم اکسیژن میشود.
برای درک بهتر تمرین بالا، این پست را مطالعه فرمایید یا در این آزمون رایگان شرکت کنید.