در واکنشهای برگشت ناپذیر که نماد واکنش آنها به صورت → میباشد، به صورت یک طرفه انجام میشوند: یعنی واکنش دهندهها تبدیل به فراوردهها میشوند، ولی فراوردهها مجدد به واکنش دهندهای تبدیل نخواهند شد، مانند واکنش سوختن متان:
CH4(g)+2O2(g)→CO2(g)+2H2O(g)
در واکنش بالا از متان (CH4) و گاز اکسیژن، گاز کربن دی اکسید و بخار آب تولید میشود، ولی از کربن دی اکسید و بخار آب، متان و گاز اکسیژن به دست نخواهد آمد، پس واکنش در جهت برگشت انجام نشده و برگشت ناپذیر است.
ولی در واکنشهای برگشت پذیر که نماد واکنش آنها به صورت ⇌ نشان میدهیم، به صورت دو طرفه انجام میشود: یعنی همان طور که واکنش دهندهها تبدیل به فراوردهها میشوند، فراوردهها هم با تولید شدن، تبدیل به واکنش دهندههای سازندۀ خود میشوند، مانند واکنش تولید آمونیاک:
N2(g)+3H2(g)⇌2NH3(g)
در واکنش بالا همان طور که از ترکیب گاز نیتروژن و گاز اکسیژن، آمونیاک (NH3) تولید میشود، آمونیاک تولیدی هم در جهت برگشت تبدیل به گازهای نیتروژن و اکسیژن خواهد شد؛ پس واکنش برگشت پذیر خواهد بود.
با توجه به اینکه واکنشهای برگشت پذیر دو طرفه بوده، و فراورده هم به واکنش دهنده تبدیل میشود پس میتوان نتیجه گرفت: در واکنشهای برگشت پذیر هیچ مادهای تمام نمیشود.
همچنین نیاز به یادآوری است: وقتی واکنشی به سمت فراورده پیش رود اصطلاحا می گوییم واکنش در جهت رفت انجام شده و برعکس، وقتی واکنشی به سمت واکنش دهندهها پیش رود، می گوییم واکنش در جهت برگشت انجام شده است:
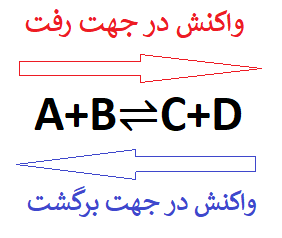
حال اگر در یک واکنش برگشت پذیر، سرعت تبدیل واکنش در جهت رفت با سرعت واکنش در جهت برگشت برابر باشد، به آن واکنش تعادلی گوییم که در پست بعدی به آن خواهیم پرداخت.
یک نظر
چون واکنش دو طرفه است در حال تولید نیز هست