زبان رایج استوکیومتری مول میباشد و مول چیزی نیست به جز تعداد 1023×6.02 عدد از هر ذره.
به طور کلی زمانی که بخواهیم در یک واکنش از یک واحد مادهای (مثل جرم یا حجم یا…) به واحد مادۀ دیگری برسیم ابتدا باید واحد مادۀ اول را به مول تبدیل کنیم، سپس از مول ماده اول به مول ماده دوم برسیم، به عبارتی تنها راه رسیدن از مادۀ اول به مادۀ دوم استفاده از مول است.
حال برای اینکه بخواهیم از مول یک ماده به مول مادۀ دیگری برسیم، باید:
1) معادلۀ شیمیایی (از نوع نمادی) را داشته باشیم.
2) معادله را موازنه کنیم (چون برای انجام استوکیومتری نیاز به ضرائب استوکیومتری مواد موجود در واکنش داریم)
3) مول یکی از مواد را داشته باشیم (تا از مول ماده اول به مول ماده دوم برسیم)
مثال: برای تهیه گاز آمونیاک طی معادلۀ شیمیایی زیر، با داشتن 6 مول گاز هیدروژن (H2)، چند مول گاز آمونیاک (NH3) تولید میشود؟ و چند مول گاز نیتروژن (N2) مصرف میشود؟
N2(g)+H2(g)→NH3(g)
پاسخ: معادلۀ شیمیایی را داریم، پس برویم سراغ موازنه:
N2(g)+H2(g)→NH3(g)
N: 2 1
H: 2 3
همان طور که میبینیم تعداد N و H در سمت واکنش دهنده و فراورده برابر نیست، و برای موازنه N باید سمت فراورده را در 2 ضرب کرده تا هر دوسمت 2 تا N داشته باشیم، در این صورت تعداد H سمت فراورده هم 6 تا میشود، پس باید H2 را هم در 3 ضرب کرده تا تعداد H در هر دو سمت برابر و موازنه شود:
N2(g)+3H2(g)→2NH3(g)
حال با موازنه شدن، داشتن مول اولیه گاز هیدروژن (که صورت سوال داده) میتوان مول تولیدی گاز آمونیاک (NH3) و مول مصرفی گاز نیتروژن (N2) را با توجه به ضرائب استوکیومتری آنها به دست آورد:
همان طور که در معادله موازنه شده میبینیم، به ازای مصرف 1 مول از گاز نیتروژن، ۲ مول گاز آمونیاک تولید میشود یا به ازای مصرف سه مول از گاز هیدروژن باز دو مول از گاز آمونیاک تولید خواهد شد، پس میتوان به صورت تناسبی گفت، وقتی مصرف 3 مول گاز هیدروژن، باعث تولید 2 مول گاز آمونیاک میشه، پس مصرف 6 مول گاز هیدروژن، چند مول گاز آمونیاک تولید میکنه؟
3mol H2 : 2mol NH3
6mol H2 : ?mol NH3
که پاسخ تناسب بالا به صورت زیر خواهد بود:
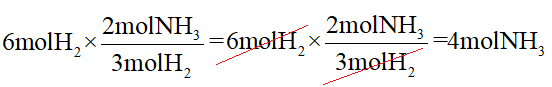
کسر بالا، به کسر مولی معروف است، که اعداد موجود در این کسر همان طور که میبینیم ضرائب استوکیومتری حاصل از موازنه مواد، است؛
کاربرد مهم کسر مولی این است که میتوانیم با استفاده از آن، از مول یک ماده، مول مادۀ دیگر را به دست آوریم، همان طور که در مثال بالا با استفاده از کسر مولی، از مول گاز هیدروژن داده شده در صورت سوال، مول گاز آمونیاک را به دست آوردیم.
فقط یه مورد را فراموش نکنیم، در زمان نوشتن کسر مولی اگر شک کردیم که مول کدام ماده را در صورت کسر بنویسیم و مول کدام ماده را در مخرج کسر، یادمان باشد که همیشه مول مادهای را در مخرج بنویسیم که قبل از کسر آن ماده را در صورت نوشتهایم، به قول کتاب شیمیوم: واحد و مادۀ صورت کسر قبلی، واحد و مادۀ مخرج کسر بعدیه. برای درک بهتر به حل قسمت دوم مثال بالا دقت کنید:
در صورت سوال گفته شده با مصرف 6 مول گاز هیدروژن چند مول گاز نیتروژن (N2) مصرف میشود، معادله هم که هست:
N2(g)+3H2(g)→2NH3(g)
پس میتوان نوشت:
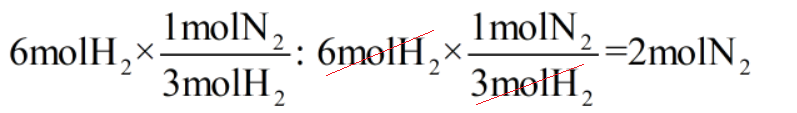
همان طور که در بالا میبینیم برای رسیدن از مول گاز هیدروژن به مول گاز نیتروژن از کسر مولی استفاده شده، که در مخرج کسر از مول گاز هیدروژن استفاده میکنیم تا با مول هیدروژن قبل از کسر خط بخورد و ساده شود و در آخر فقط مول مادهای که سوال از ما میخواهد باقی بماند (یعنی مول نیتروژن)