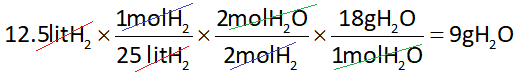استوکیومتری مسائل حجمی (شرایط غیرSTP)
گازها در شرایط غیر STP (دما و فشار به ترتیب برابر با 0 درجه سانتیگراد و 1 اتمسفر نباشند) دارای حجم مولی غیر از 22.4lit/mol خواهند بود، زیرا با تغییر دما و فشار، حجم گازها نیز تغییر میکند.
در شرایط غیر STP اغلبا حجم مولی گاز در سوال داده میشود و با استفاده از آن میتوان سوال را مانند قبل جلو برد، با این تفاوت که برای قسمت حجم مولی، به جای استفاده از 22.4lit/mol از عددی استفاده میکنیم که صورت سوال داده است.
مثال: از واکنش ۱۲.۵ لیتر گاز هیدروژن چند گرم آب تولید میشود؟ (حجم مولی گاز هیدروژن 25lit/mol) (H:1g/mol O:16g/mol)
H2(g)+O2(g)→H2O(l)
ابتدا موازنه بودن واکنش را بررسی میکنیم:
H2(g)+O2(g)→H2O(l)
H: 2 2
O: 2 1
برای موازنه شدن اتم اکسیژن، سمت فراورده باید در 2 ضرب شود تا تعداد اکسیين دو طرف برابر شود، که در این صورت اتم هیدروژن سمت فراورده هم 2 برابر میشود، پس H2 را نیز در 2 ضرب میکنیم تا اتمهای در طرف موازنه شوند:
2H2(g)+O2(g)→2H2O(l)
حالا بریم سراغ استوکیومتری:
با توجه به صورت سوال چون حجم مولی گاز هیدروژن عددی غیر از 22.4lit/mol است، پس شرایط غیرSTP محسوب میشود، ولی تفاوتی در حل سوال ندارد. یعنی همانند قبل: با استفاده از حجم مولی گاز هیدروژن (25lit/mol) از حجم گاز هیدروژن به یک مول آن میرسیم و با استفاده از کسر مولی، از مول گاز هیدروژن به مول آب (H2O) میرسیم و از طریق جرم مولی آب به جرم آن میرسیم؛ پس در ابتدا نیاز به جرم مولی آب داریم:
H2O: 2(1)+16=18g/mol
و کسرهای استوکیومتری به صورت زیر خواهد بود:
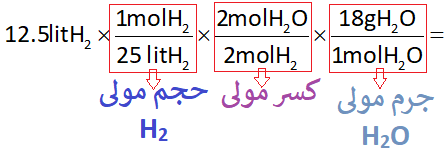
که با ساده کردن کسرها به پاسخ سوال میرسیم: