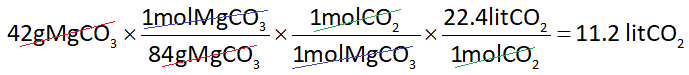به یاد داشته باشیم که ماده و واحد صورت هر کسر با ماده و واحد مخرج کسر بعدی باید یکی باشد تا با هم خط بخورند و ساده شوند.
مثال: از تجزیه 42g منیزیم کربنات چند لیتر گاز در شرایط STP آزاد میشود؟ Mg=24g/mol, C:12g/mol, O:16g/mol
MgCO3(s)→MgO(s)+CO2(g)
پاسخ: در ابتدا از موازنه بودن واکنش مطمئن میشویم که با وجود برابر بودن اتمها در دو سمت این اطمینان حاصل میشود.
بریم سراغ استوکیومتری:
با توجه به توضیحات ابتدای مطلب ب توجه به شرایط STP، از جرم مول MgCO3 با استفاده از جرم مولی آن به مول آن میرسیم و با استفاده از کسر مولی از به مول گاز CO2 میرسیم و از طریق حجم مولی استاندارد گازها (22.4lit/mol) از مول گاز CO2 به حجم آن میرسیم، پس در ابتدا نیاز به جرم مولی MgCO3 داریم: MgCO3:24+12+3(16)=84g/mol
در نتیجه کسرهای استوکیومتری به صورت زیر خواهد بود:
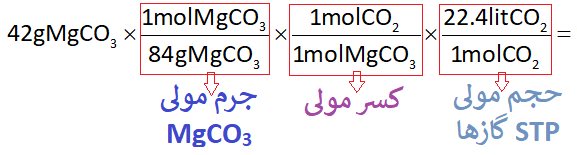
در آخر با ساده کردن کسرها به پاسخ سوال میرسیم: