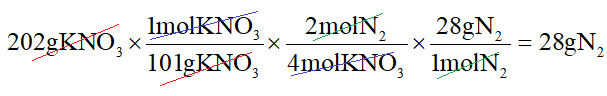به یاد داشته باشیم که ماده و واحد صورت هر کسر با ماده و واحد مخرج کسر بعدی باید یکی باشد تا با هم خط بخورند و ساده شوند.
مثال: از تجزیه 202g پتاسیم نیترات (KNO3) در دمای بالا، چند گرم گاز نیتروژن آزاد میشود؟
(KNO3:101g/mol, N2:28g/mol)
KNO3(s)→K2O(s)+O2(g)+N2(g)
پاسخ: با داشتن واکنش ابتدا آن را موازنه میکنیم:
KNO3(s)→K2O(s)+O2(g)+N2(g)
K: 1 2
N: 1 2
0: 3 3
برای موازنه اکسیژن را در آخر موازنه میکنیم (زیرا بیشتر از بقیه اتمها تکرار شده است)، تعداد K سمت فراورده دو برابر واکنش دهنده هست، پس KNO3 رو در ۲ ضرب میکنیم، و O2 را در 3.5 ضرب میکنیم، برای اینکه ضریب O2 از حالت کسری خارج شود، هم مواد را در 2 ضرب میکنیم که حالت موازنه شده واکنش به صورت زیر میشود:
4KNO3(s)→2K2O(s)+5O2(g)+2N2(g)
حال سراغ استوکیومتری میرویم:
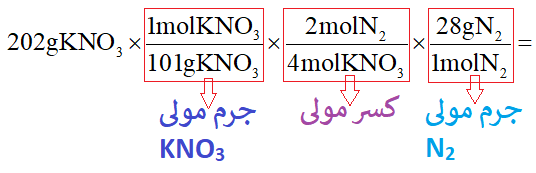
همان طور که در ابتدای همین مطلب گفته شد، ابتدا با استفاده از جرم مولی مادۀ داده شده (KNO3) به مول آن میرسیم و از طریق کسر مولی از مول مادۀ اول به مول مادۀ دوم (N2) میرسیم و در نهایت با استفاده از جرم مولی مادۀ دوم به جرم آن میرسیم، به صورت زیر:
در آخر با ساده کردن کسرها جرم تولیدی گاز نیتروژن به ازای مصرف 202g پتاسیم کربنات به دست میآوریم: