به عبارتی سرعت مصرف واکنش دهندهها و سرعت تولید فراوردهها، با ضریب استوکیومتری آنها رابطۀ مستقیم دارد، برای درک بهتر به واکنش زیر دقت کنید:
در واکنش بالا، ضریب استوکیومتری فراورده، 2 برابر ضریب استوکیومتری واکنش دهنده است، پس میتوان نتیجه گرفت سرعت تولید فراورده نیز 2 برابر سرعت مصرف واکنش دهنده خواهد بود، مطابق نمودار زیر:
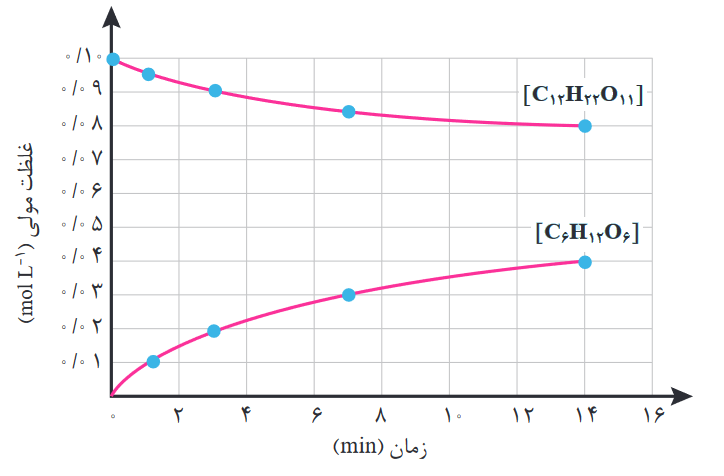
همان طور که در نمودار بالا مشاهده میکنیم، منحنی تولید فراورده در زمان برابر با واکنش دهنده، شیب بیشتری نسبت به منحنی واکنش دهنده دارد، و شیب منحنی غلظت-زمان، همان سرعت است.
مثال: در واکنش فرضی زیر بیشترین سرعت مربوط به کدام ماده است؟
2A+B→3C+D
پاسخ: با توجه به ضرائب استوکیومتری: سرعت: C>A>B=D
توضیح: بیشترین سرعت مربوط به مادۀ C بوده، چون بیشترین ضریب استوکیومتری را دارد (ضریب استوکیومتری مادۀ C برابر با 3 هست) و بعد از آن مادۀ A با ضریب استوکیومتری 2 و کمترین را سرعت مواد B و D دارند، (با ضرائب استوکیومتری 1)
البته فراموش نکنیم که مادۀ C و D فراورده هستند و علامت سرعت آنها، قرینه مواد A و B میباشد، زیرا فراوردهها در حال تولید شدن و افزایش هستند و واکنش دهندهها در حال مصرف شدن و کم شدن هستند، مثلا نسبت سرعت مادۀ C به مادۀ A برابر است با:
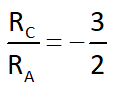
علامت منفی به این دلیل است که طبق توضیح بالا، ماده C فراورده و ماده A واکنش دهنده است.