به عبارتی با وجود آب سخت، صابون قدرت پاک کنندگی خود را طبق توضیح بالا از دست میدهد و کف نمیکند.
زیرا میزان کف کردن صابون با انحلال پذیری و پاک کنندگی آن رابطه مستقیم دارد.
پس میتوان گفت در حضور آب سخت، محصول صابون و یونهای کلسیم و منیزیم، به جای محلول شدن در آب و کف کردن، رسوب میکنند، طبق واکنش زیر:
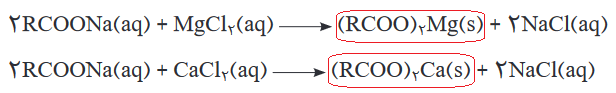
همان طور که در فراورده واکنش ها مشاهده میکنیم فاز تشکیل شده حاصل از واکنش صابون با مواد حاوی یونهای کلسیم و منیزیم، جامد (رسوب) است و در آب محلول نمیباشند؛ و از نگاه بیننده صابون کف نمیکند؛ در نتیجه برای آب سخت نیاز به پاک کنندههای دیگری پیدا میکنیم که اصطلاحا به آنها پاک کنندههای غیر صابونی گویند و در پست بعدی به آن خواهیم پرداخت.
سوال: با توجه به فاز مواد در واکنشهای بالا کدوم مواد محلول در آب هستن و کدوم مواد جامد (رسوب) هستن؟
2 نظر
آیا صابون R_COONH4 هم در آب این گونه عمل میکند؟
بله، با وجود این صابون هم آب سخت، کف نمیکند، زیرا مجددا RCOOMg تشکیل میشود که نامحلول در آب است و به عبارتی رسوب میکند.